阿斯利康和第一三共撤回 TROP2-DXD提交的上市申请

撤回 MAA 的决定是根据欧洲药品管理局 (EMA) 人用药品委员会的反馈做出的。阿斯利康和第一三共将继续努力 将 datopotamab deruxtecan 带给欧盟的肺癌患者,使他们能够从中受益,并致力于通过我们强大的临床开发计划释放这种药物在肺癌治疗中的潜力,该计划包括在不同肺癌环境中进行的七项关键试验。
阿斯利康和第一三共基于TROPION-Breast01三期临床试验在欧盟提出的 datopotamab deruxtecan 用于治疗激素受体 (HR) 阳性、HER2 阴性转移性乳腺癌的申请仍在审查中。
Datopotamab deruxtecan 是一种专门设计的 TROP2 导向 DXd 抗体药物偶联物 (ADC),由第一三共发现,并由阿斯利康和第一三共联合开发。
阿斯利康在2024 WCLC公布TROPION-Lung01临床研究,同时也在ASCO杂志上发表文章“Datopotamab Deruxtecan Versus Docetaxel for Previously Treated Advanced or Metastatic Non–Small Cell Lung Cancer: The Randomized, Open-Label Phase III TROPION-Lung01 Study”,公开其临床数据。
该临床研究共有299名患者和305名患者分别被随机分配接受Dato-DXd或多西他赛治疗。Dato-DXd组的中位无进展生存期(PFS)为4.4个月(95% CI, 4.2至5.6),多西他赛组为3.7个月(95% CI, 2.9至4.2)(危险比 [HR], 0.75 [95% CI, 0.62至0.91];P = 0.004)。中位总生存期(OS)分别为12.9个月(95% CI, 11.0至13.9)和11.8个月(95% CI, 10.1至12.8)(HR, 0.94 [95% CI, 0.78至1.14];P = 0.530)。未达到统计学意义。
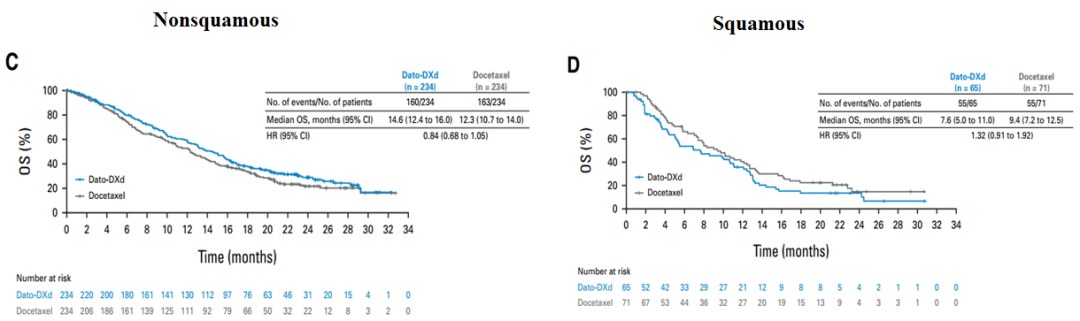
在预设的非鳞状组织学亚组中,中位PFS分别为5.5个月对比3.6个月(HR, 0.63 [95% CI, 0.51至0.79]),中位OS分别为14.6个月对比12.3个月(HR, 0.84 [95% CI, 0.68至1.05])。在鳞状组织学亚组中,中位PFS分别为2.8个月对比3.9个月(HR, 1.41 [95% CI, 0.95至2.08]),中位OS分别为7.6个月对比9.4个月(HR, 1.32 [95% CI, 0.91至1.92])。
(转自:抗体圈)